Tiêm Filler đã trở thành một phương pháp rất phổ biến để trẻ hóa làn da mặt, bao gồm cả khu vực quanh mắt. Trong những năm gần đây, các sản phẩm chứa Polynucleotide (PN) mới đã được áp dụng cho mục đích thẩm mỹ. Nghiên cứu dưới đây so sánh hiệu quả của Polynucleotide và Hyaluronic Acid trong quá trình trẻ hóa vùng quanh mắt: một nghiên cứu ngẫu nhiên, mù đôi, chia đôi khuôn mặt.
GIỚI THIỆU
Quá trình lão hóa da bao gồm những thay đổi về cả chất lượng lẫn số lượng. Một số đặc điểm chính của da lão hóa là sự mất độ đàn hồi, giảm độ dày của biểu bì và hàm lượng collagen, gia tăng nếp nhăn và tổn thương sắc tố (1). Lão hóa da ảnh hưởng to lớn tới giao tiếp xã hội, trong những năm gần đây, các phương pháp mới liên tục được phát triển để khắc phục tình trạng này. Filler da mặt đã được sử dụng rộng rãi như một thủ thuật xâm lấn tối thiểu nhằm trẻ hóa da. Trong số các sản phẩm làm đầy, Hyaluronic Acid (HA) là phổ biến nhất và tương đối an toàn (2–4).
Trong những năm gần đây, một hoạt chất filler dưỡng da mới là Polynucleotide tinh khiết (PN) có nguồn gốc từ tế bào cá hồi. PN là chuỗi dài >13 monome nucleotide liên kết cộng hóa trị với trọng lượng phân tử cao lên đến 8000 kDa và cấu trúc nhớt đàn hồi. Một số nghiên cứu đã chỉ ra rằng PN kích thích sự phát triển của tế bào (5,6) và hỗ trợ quá trình lành thương (7,8). PN tạo dựng khung đỡ cho quá trình tái tạo collagen và ma trận ngoại bào (ECM) (9,10). PN chuỗi dài, bao gồm PN với nồng độ 20mg/mL, được phát triển để tiêm vào lớp hạ bì. Park và cộng sự (11) đã ghi nhận rằng việc tiêm PN là một phương pháp hiệu quả và an toàn để điều trị trẻ hóa trong những ca lâm sàng.
Đối với việc trẻ hóa vùng quanh hốc mắt, HA có khả năng làm đầy tạm thời và có thể tiêm tan, được ưa chuộng hơn nhằm đạt được hiệu quả thẩm mỹ tự nhiên và giảm thiểu biến chứng. Do đó, trong nghiên cứu này, chúng tôi đã đánh giá hiệu quả và tính an toàn của việc tiêm PN để trẻ hóa vùng quanh hốc mắt (bao gồm vết chân chim và vùng dưới hốc mắt) so với việc tiêm chất làm đầy HA.
PHƯƠNG PHÁP
Nghiên cứu này đã được Hội đồng Đánh giá Thể chế của Trung tâm Y tế Asan phê duyệt và tuân thủ các hướng dẫn của Tuyên bố Helsinki năm 1975. Tất cả bệnh nhân đều đã có sự đồng ý với thông tin trước khi tham gia nghiên cứu, bao gồm cả mẫu đơn đồng ý chụp ảnh đã được ký trước khi ghi danh.
SỐ LƯỢNG NGHIÊN CỨU
Từ tháng 6 năm 2017 đến tháng 11 năm 2017, những cá nhân mong muốn điều trị trẻ hóa vùng quanh hốc mắt đã được ghi danh vào nghiên cứu. Những người trong độ tuổi từ 25 đến 70 được chọn đưa vào nghiên cứu này. Những cá nhân đồng ý hạn chế các phương pháp điều trị khác liên quan đến nếp nhăn, các rối loạn về da, nhiễm trùng vết thương trên mặt, tiền sử sẹo lồi hoặc sẹo phì đại, và sẹo kéo dài hơn 1 năm mặt hoặc sẹo trên vùng điều trị, sử dụng liệu pháp chống đông máu (trừ liệu pháp aspirin liều thấp (100mg; tối đa 300mg/ngày)) trong vòng hai tuần, sử dụng các tác nhân tại chỗ (tức là steroid và retinoid, trừ mỹ phẩm) trên mặt trong vòng bốn tuần, sử dụng liệu pháp chống nhăn hoặc trị mụn trên mặt trong vòng 3 tháng, sử dụng liệu pháp trẻ hóa khuôn mặt hoặc phẫu thuật thẩm mỹ (bao gồm tiêm độc tố botulinum hoặc tiêm chất làm đầy) trong vòng sáu tháng qua, tiêm chất làm đầy vĩnh viễn trên mặt và tham gia vào thử nghiệm thuốc hoặc nghiên cứu điều tra khác trong vòng 30 ngày.
NGUYÊN LIỆU NGHIÊN CỨU
Rejuran (Pharmaresearch Products, Inc., Seoul, Hàn Quốc), một sản phẩm chứa chất lỏng trong suốt gồm 20 mg/ml PN, đã được sử dụng trong nghiên cứu. Yvoire-Hydro (LG Life Sciences, Seoul, Hàn Quốc), chứa HA không liên kết chéo nồng độ cao và dung dịch đệm phosphate Dulbecco (DPBS; Join Bio-Innovation, Seoul, Hàn Quốc), đã được sử dụng làm thiết bị kiểm soát.
ĐỀ CƯƠNG NGHIÊN CỨU VÀ QUY TRÌNH ĐIỀU TRỊ
Sau các lần thăm khám sàng lọc, các đối tượng được phân chia ngẫu nhiên vào nhóm nghiên cứu (PN; Rejuran) và nhóm đối chứng (HA; Yvoire-Hydro) để tiêm vào bên phải hoặc bên trái của khuôn mặt sau khi đánh giá ban đầu (tuần [W] 0). Sau đó, hai nhà nghiên cứu (Ye Jin Lee và You Jin Lee) tiêm ba lần với khoảng cách hai tuần (W0, W2 và W4). Sau đó, bệnh nhân đến phòng khám để đánh giá vào W10, W16 và W28 sau lần điều trị ban đầu.
Trước khi tiêm, thuốc gây tê tại chỗ lidocaine và kem prilocaine được bôi lên vùng điều trị trong 30 phút. Vùng điều trị bao gồm vết chân chim và vùng dưới hốc mắt nối liền cánh mũi và khóe mắt bên. Sau khi làm sạch bằng chlorhexidine, tất cả các đối tượng đều được điều trị PN ở một bên và HA ở bên đối diện của khuôn mặt (tối đa 1ml). Tất cả các phương pháp điều trị đều được thực hiện bằng kỹ thuật tiêm dưới da, các mũi tiêm 0,02ml PN cách nhau 0,5–1cm theo hình dạng lưới. Sử dụng ống tiêm 1ml với kim cỡ 33 (kim JBP Nano). Các đối tượng được theo dõi trong 30 phút sau khi điều trị để phát hiện phản ứng dị ứng cấp tính.
Phương pháp ngẫu nhiên và mù đôi
Một bảng số ngẫu nhiên đã được sử dụng để phân bổ ngẫu nhiên. Mỗi đối tượng được phân bổ ngẫu nhiên liên tiếp vào công thức PN hoặc HA trên mỗi nửa mặt tại thời điểm ghi danh. Việc chỉ định công thức trái/phải được niêm phong trong phong bì. Những người tham gia và nhà nghiên cứu tham gia vào các đánh giá lâm sàng đã bị giữ bí mật về việc áp dụng PN hoặc HA lên phía mặt nào. Hai bác sĩ da liễu (HTK và SHP) không có mặt trong suốt quá trình thực hiện đánh giá lâm sàng.
Đánh giá hiệu quả hoạt động
Hai bác sĩ da liễu độc lập (HTK và SHP) đã đánh giá kết quả bằng thang điểm cải thiện thẩm mỹ toàn cầu (GAIS) dựa trên các bức ảnh ở W10, W16 và W28 theo thang điểm tứ phân vị được định nghĩa như sau: -1: nghiêm trọng hơn; 0: không thay đổi; 1: cải thiện; 2: cải thiện nhiều. Đối với đánh giá chủ quan, các đối tượng sử dụng thang điểm tương tự thị giác (VAS) với điểm từ 0 đến 100 (không cải thiện đến cải thiện rất tốt) tại W10, W16 và W28. Mức độ hydrat hóa của da và độ đàn hồi của da được đo bằng máy đo độ cong giác mạc (CM 825; Courage & Khazaka, Đức) tại thời điểm ban đầu, W4, W10, W16 và W28. Phép đo được thực hiện bởi một nhà nghiên cứu (YSM), và các vị trí đo là các điểm mà đường giữa đồng tử gặp cánh mũi ở cả hai bên. Giá trị trung bình của 5 phép đo bằng máy đo góc đã được ghi lại. Mức độ sần (12) và thể tích lỗ chân lông (13) đã được đo bằng hệ thống chụp ảnh ba chiều (3D) Antera (Miravex, Dublin, Ireland). Độ dày của da đã được đo bằng máy quét da (DUB-USB; Taberna pro med- icum, Đức) ở mức cơ bản, W16 và W28.
Tất cả các tác dụng phụ (AE), bao gồm đau, sưng, cứng, bầm tím và ngứa, tại khu vực điều trị xảy ra trong quá trình nghiên cứu đều được đánh giá thông qua phỏng vấn những người tham gia và quan sát phản ứng của da tại mỗi lần khám.
Phân tích dữ liệu thống kê
Phân tích thống kê được thực hiện dựa trên ý định điều trị và sử dụng phần mềm SPSS phiên bản 20.0 (IBM Corp., Armonk, NY). Giá trị p < .05 được coi là có ý nghĩa thống kê. Dữ liệu về điểm VAS, điểm GAIS, độ đàn hồi của da, độ ẩm, độ sần, thể tích lỗ chân lông và độ dày được phân tích để xác định ý nghĩa thống kê thông qua mô hình hỗn hợp tuyến tính (tức là mô hình mẫu hiệp phương sai). Mối quan hệ giữa các phép đo cutometer (tức là R2, R5 và R7) và camera Antera 3D (tức là độ sần của da và kích thước lỗ chân lông) được xác định bằng cách sử dụng thử nghiệm hệ số tương quan Pearson.
KẾT QUẢ
Đối tượng và hiệu quả
Trong số 34 đối tượng được sàng lọc, 30 đối tượng đã được phân bổ ngẫu nhiên và 27 đối tượng đã được điều trị. 27 đối tượng được điều trị đã được đánh giá tại W4, W10 và W16, và 23 đối tượng đã được đánh giá tại W28 (Hình 1).
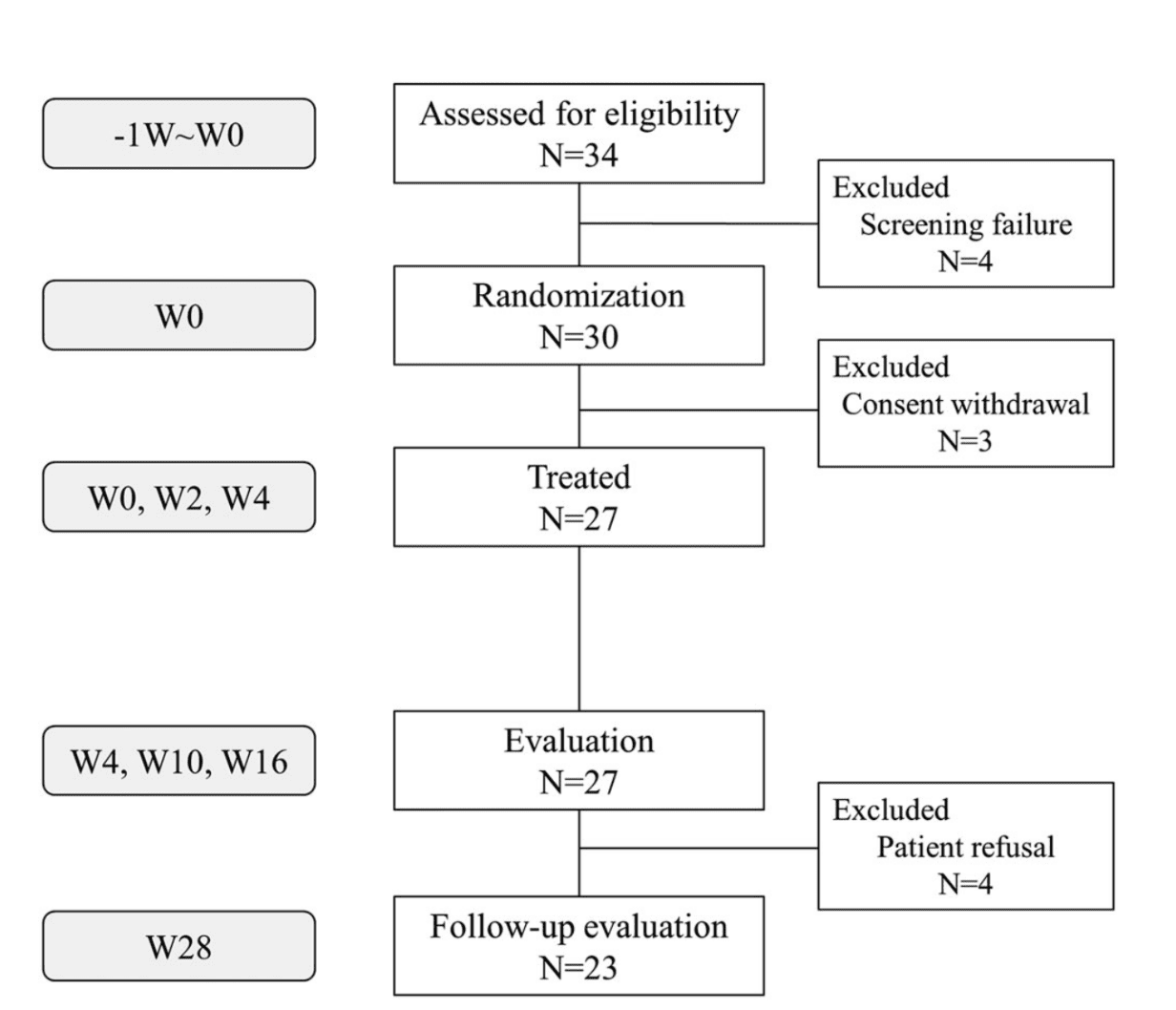
Hình 1: Sơ đồ các đối tượng tham gia nghiên cứu.
Tất cả các đối tượng đều là phụ nữ với độ tuổi trung bình là 48,78 năm (dao động: 37–62 năm). Tám đối tượng ở độ tuổi 35–44, 10 người ở độ tuổi 45–54 và chín người ở độ tuổi 55–64. Điểm GAIS cao hơn ở nhóm PN so với nhóm HA ở mức ¼ .0398). Ngược lại, điểm VAS không cho thấy sự khác biệt đáng kể giữa các nhóm; nó giảm dần theo thời gian (Hình 2–4). 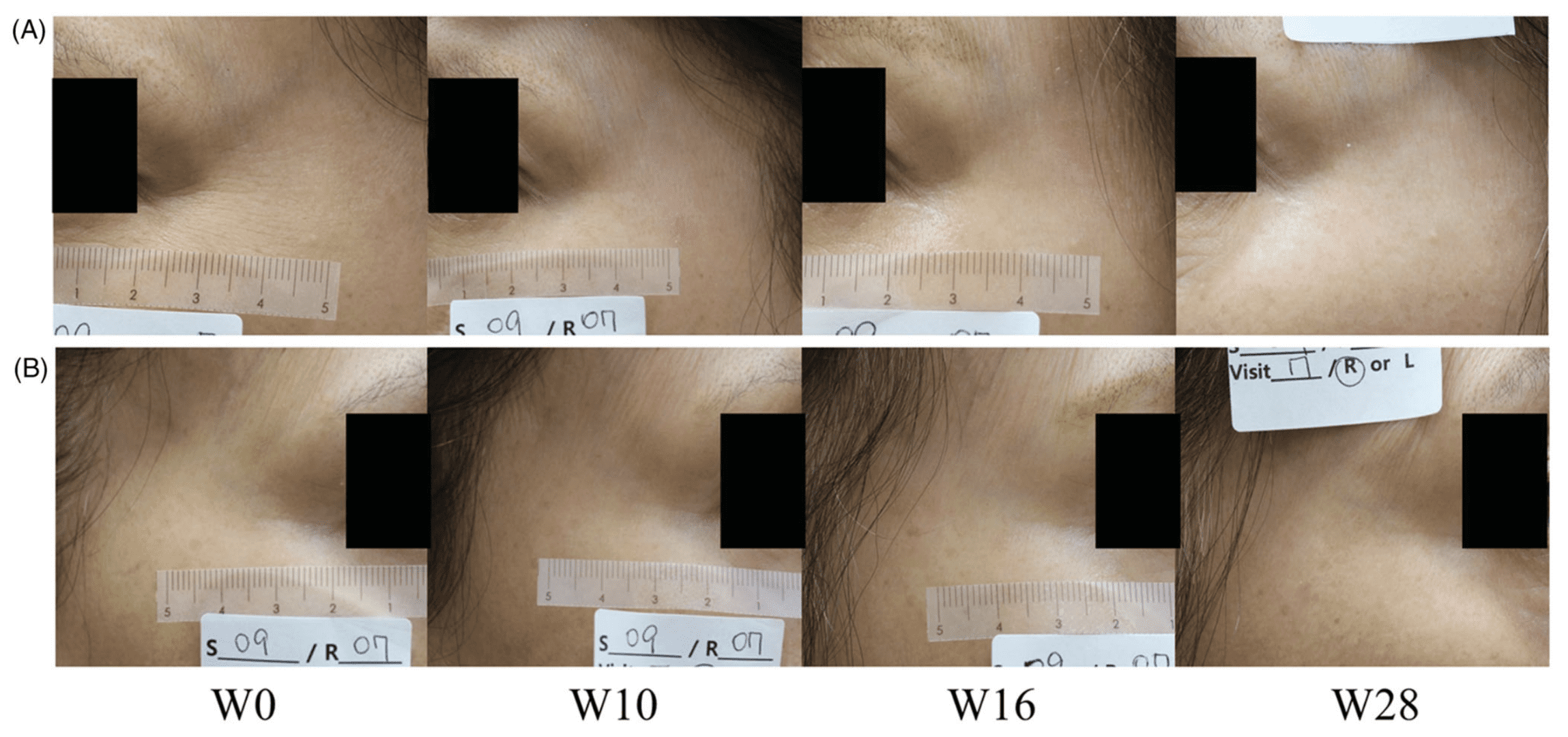
Hình 2. Ảnh chụp lâm sàng của một phụ nữ 60 tuổi ở thời điểm ban đầu và tuần thứ 10, 16 và 24. Những thay đổi về vết chân chim và kết cấu da ở bên được điều trị bằng Polynucleotide (A) và chất làm đầy Hyaluronic Acid (B) được hiển thị.
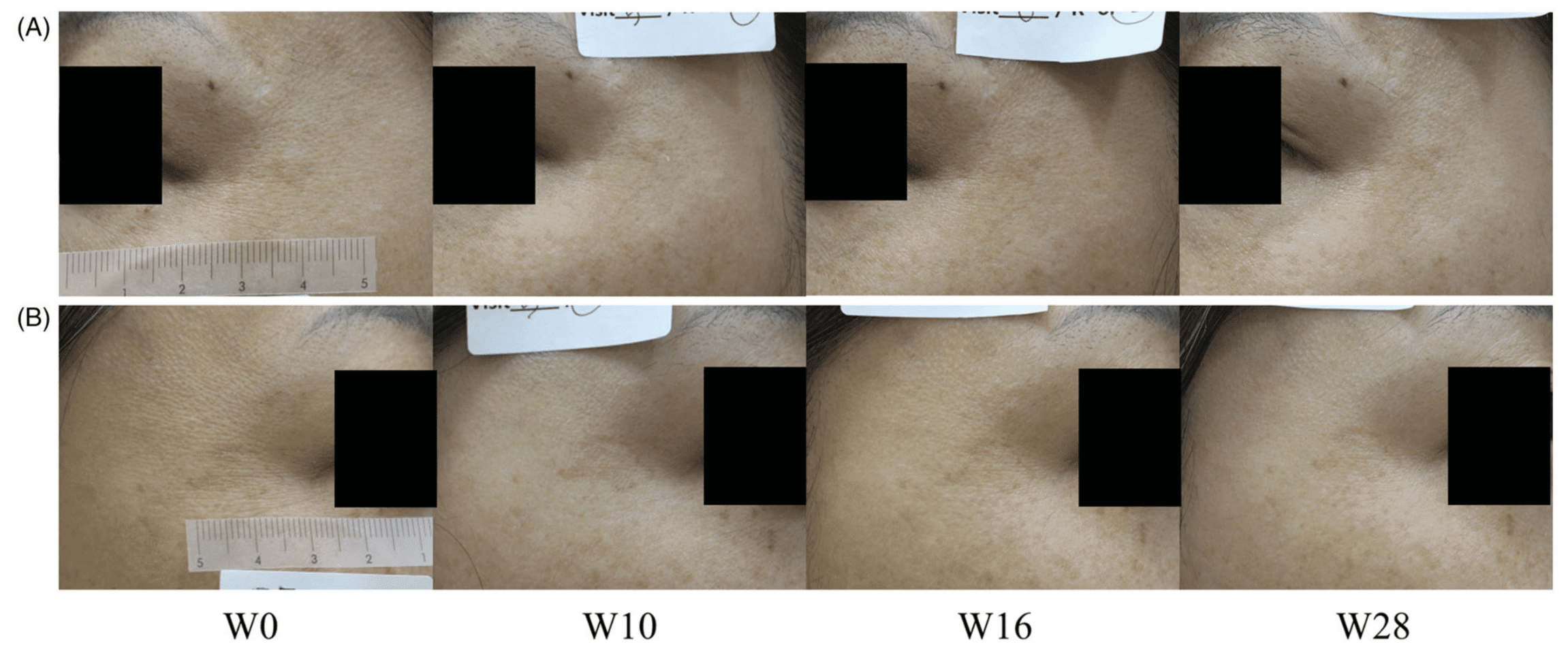
Hình 3. Ảnh chụp lâm sàng của một phụ nữ 40 tuổi ở thời điểm ban đầu và tuần thứ 10, 16 và 24. Những thay đổi về vết chân chim và kết cấu da ở bên được điều trị bằng Hyaluronic Acid (A) và chất làm đầy Polynucleotide (B) được hiển thị.
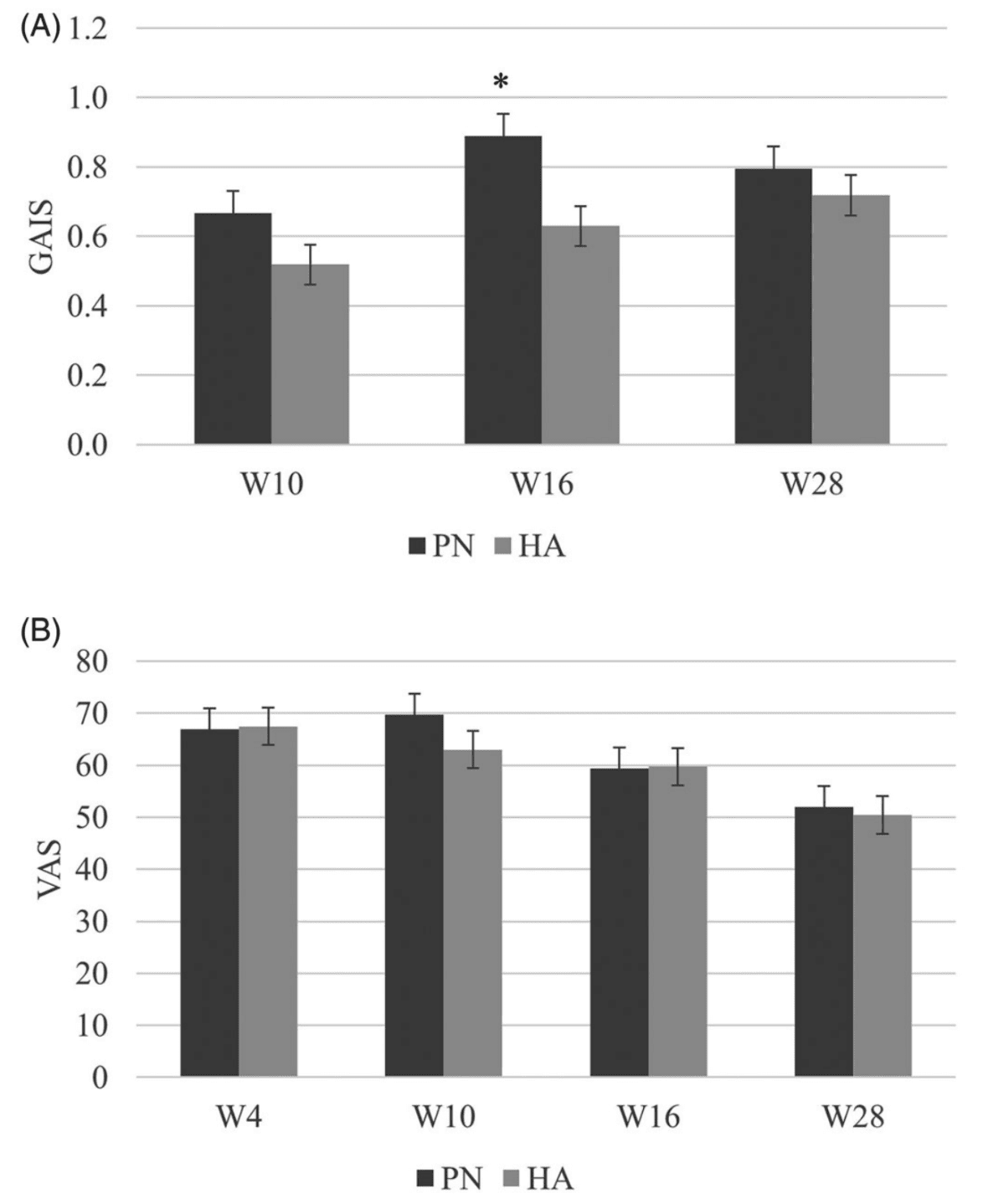
Hình 4. (A) Điểm cải thiện thẩm mỹ toàn diện (GAIS) và (B) điểm tương tự thị giác (VAS) của nhóm Polynucleotide (PN) và Hyaluronic Acid (HA) (p <.05).
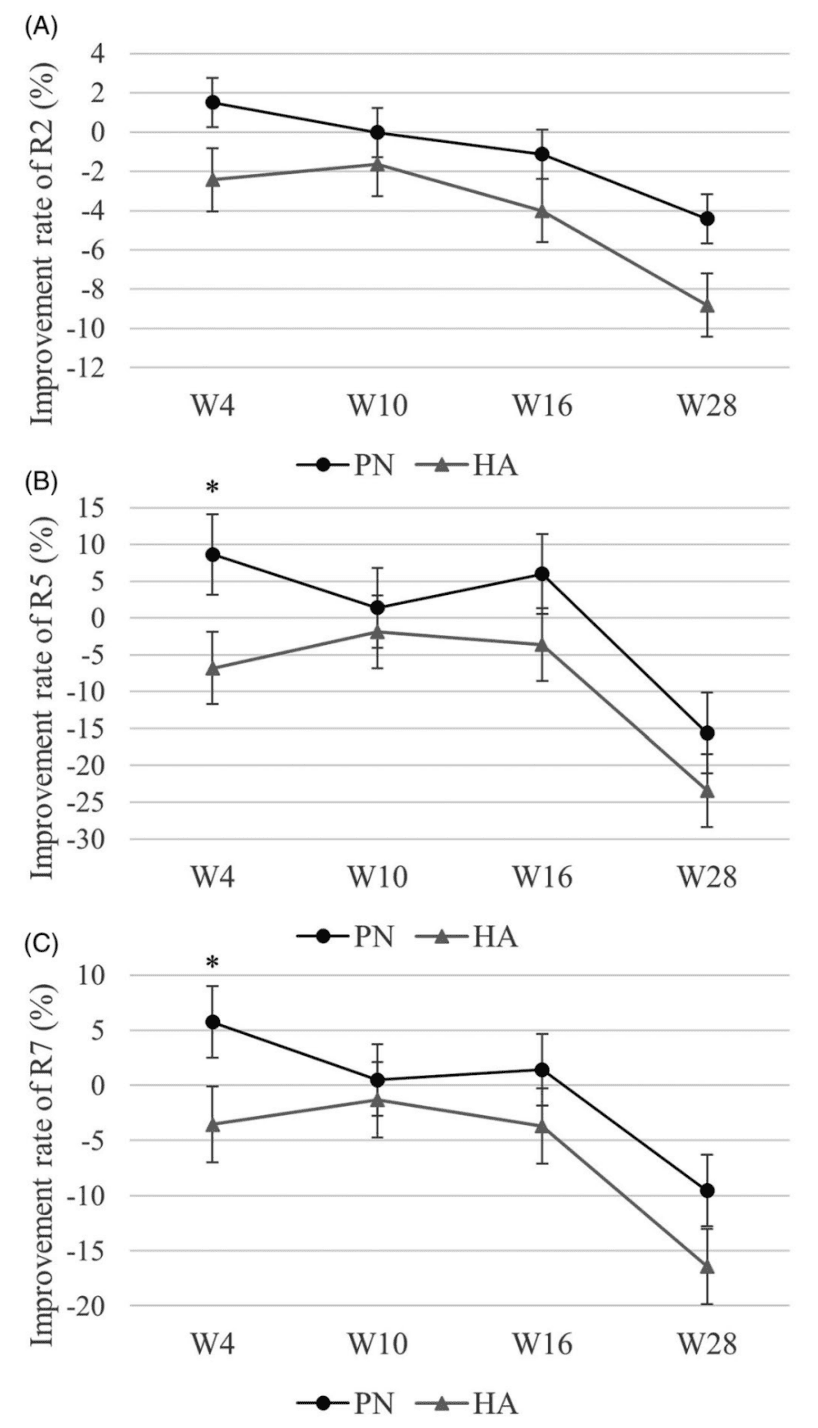
Hình 5. Tỷ lệ cải thiện của (A) R2, (B) R5 và (C) R7 trong nhóm Polynucleotid (PN) và Hyaluronic Acid (HA) (p <.05).
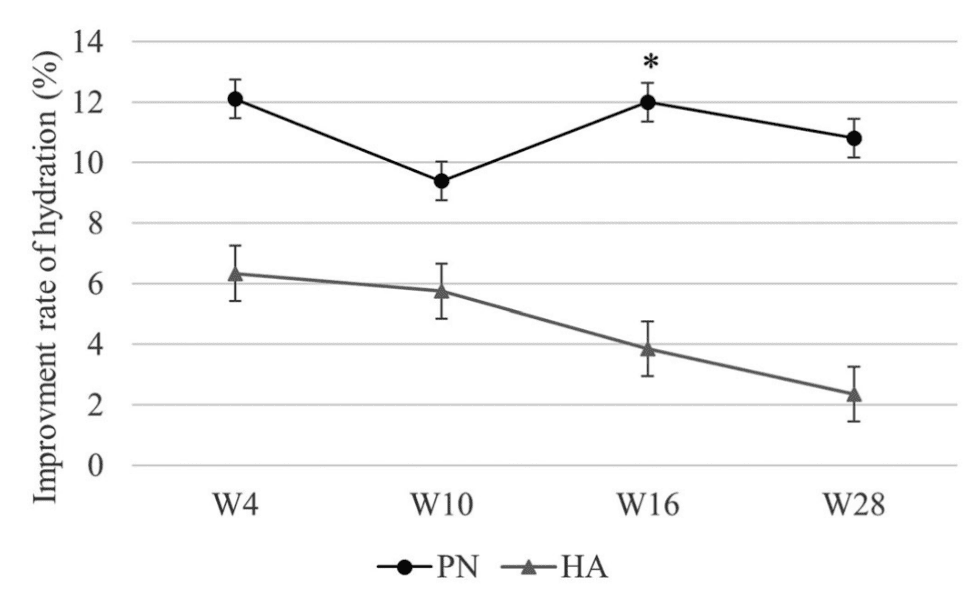
Hình 6. Tỷ lệ cải thiện hydrat hóa trong nhóm Polynucleotide (PN) và Hyaluronic Acid (HA) (p <.05).
Độ đàn hồi và độ ẩm của da
Hình 5 cho thấy tỷ lệ cải thiện độ đàn hồi của da, được biểu thị bằng R2, R5 và R7. Tỷ lệ cải thiện của R2, R5 và R7 đối với cả nhóm PN và HA đều giảm theo thời gian (R2: p = .0034, R5: p < .0001 và R7: p < .0001), cho thấy sự tương tự mẫu. Mối quan hệ tích cực giữa tỷ lệ cải thiện của R2, R5 và R7 đã được quan sát thấy trong phân tích tương quan (r> 0,5, p < .0001). Sự thay đổi trong tỷ lệ cải thiện của R2, R5 và R7 theo thời gian không cho thấy bất kỳ sự khác biệt đáng kể nào giữa nhóm PN và HA (p = .853, p = .4427 và p = .48, tương ứng). Tuy nhiên, khi hiệu ứng thời gian được cố định, tỷ lệ cải thiện của R2, R5 và R7 trong nhóm PN cao hơn trong nhóm HA (p =.0133, p = .0025 và p = .003). Tỷ lệ cải thiện của R5 và R7 trong nhóm PN cao hơn so với nhóm HA tại W4 (R5: p = .0046 và R7: p =.0087)
Mặc dù sự thay đổi trong tỷ lệ cải thiện hydrat hóa theo thời gian không cho thấy bất kỳ sự khác biệt đáng kể nào giữa nhóm PN và HA (p = .8281), tỷ lệ cải thiện của hydrat hóa trong nhóm PN cao hơn so với HA (p = .0043; Hình 6). Tỷ lệ cải thiện hydrat hóa trong nhóm PN cao hơn nhóm HA ở W16 (p=.0486).
Độ sần và thể tích lỗ chân lông
Sự thay đổi trong tỷ lệ cải thiện độ sần da theo thời gian ở nhóm PN cao hơn nhóm HA (p=.0247). Tỷ lệ cải thiện độ sần ở nhóm PN tăng theo thời gian, trong khi ở nhóm HA lại giảm. Tỷ lệ cải thiện độ sần ở nhóm PN cao hơn ở nhóm HA tại W28 (p=.0206, Ảnh 7(A)).
Sự thay đổi trong tỷ lệ cải thiện thể tích lỗ chân lông theo thời gian không cho thấy bất kỳ sự khác biệt đáng kể nào giữa nhóm PN (p = 0.0568). Tuy nhiên, khi hiệu ứng thời gian được cố định, tỷ lệ cải thiện thể tích lỗ chân lông trong nhóm PN là (p = 0.0028). Sự cải thiện tỷ lệ cải thiện thể tích lỗ rỗng trong nhóm PN cao hơn nhóm HA tại W16 (p=.0091) và W28 (p= .0045; Hình 7(B)). Cải thiện độ sần da và kích thước lỗ chân lông cũng được quan sát thông qua sử dụng máy Antera 3 (Hình 7(C,D)).
Một mối quan hệ tích cực đã được quan sát thấy giữa tỷ lệ cải thiện độ sần và thể tích lỗ chân lông trong phân tích tương quan (W10: r =0,60698, p < .0001; W16: r = 0,60448, p < .0001; và W28: r = 0,80569, p < .0001).
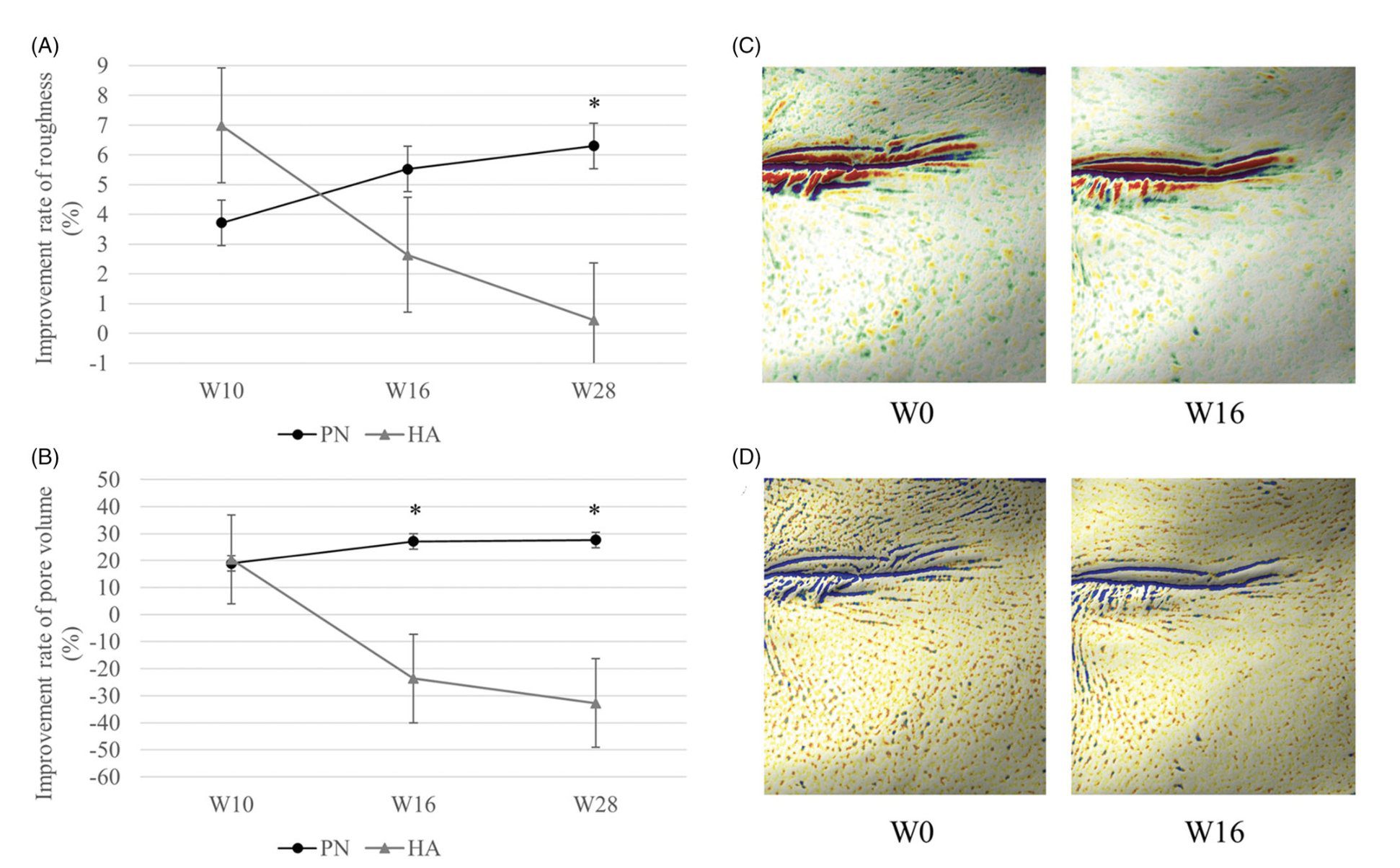
Hình 7: Tỷ lệ cải thiện của (A) độ sần nhám và (B) thể tích lỗ chân lông trong các nhóm sử dụng Polynucleotide (PN) và Axit Hyaluronic (HA) (p < 0,05). Hình ảnh cải thiện của (C) độ sần và (D) thể tích lỗ chân lông ở một phụ nữ 44 tuổi được điều trị bằng chất làm đầy PN, được quan sát bằng Antera 3D, tại thời điểm ban đầu và sau 16 tuần.
Mật độ da hạ bì
Sự thay đổi về tỷ lệ cải thiện mật độ da hạ bì theo thời gian không cho thấy bất kỳ sự khác biệt đáng kể nào giữa nhóm PN (Polynucleotide) và nhóm HA (Axit Hyaluronic) (p = 0,8884). Hơn nữa, khi cố định yếu tố thời gian, tỷ lệ cải thiện mật độ da hạ bì cũng không cho thấy sự khác biệt có ý nghĩa giữa các nhóm (p = 0,0986; Hình 8(A)). Hình 8(B) cho thấy sự gia tăng mật độ da hạ bì, được quan sát bằng cách sử dụng máy quét da.
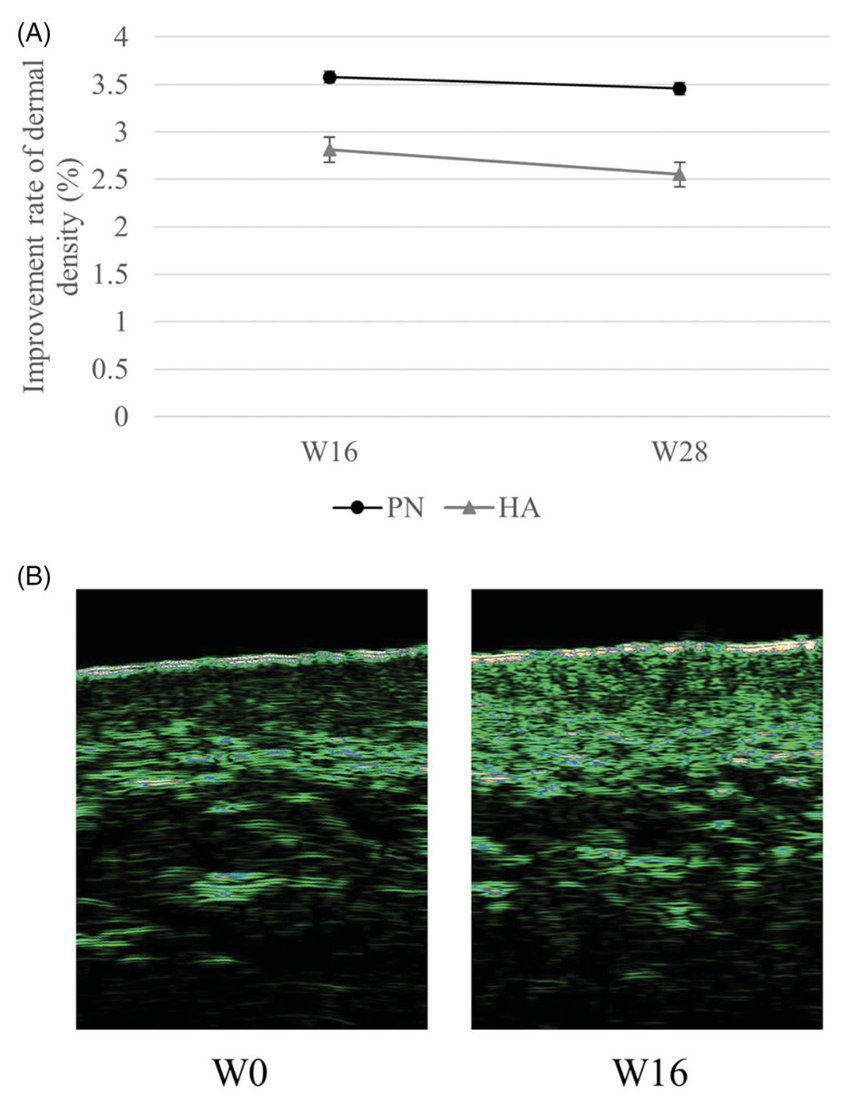
Hình: Hình 8. (A) Tỷ lệ cải thiện mật độ da ở các nhóm Polynucleotide (PN) và Hyaluronic acid (HA). (B) Sự gia tăng mật độ da ở một phụ nữ 44 tuổi được điều trị bằng chất làm đầy PN, được quan sát bằng cách sử dụng máy quét da, từ thời điểm ban đầu và sau 16 tuần.
BÀN LUẬN
Hiệu quả của PN đối với trẻ hóa da đã được so sánh với HA trong một nghiên cứu đối chứng mù đôi, chia nửa mặt. Đầu tiên, các thang đo chủ quan không cho thấy sự khác biệt đáng kể giữa hai nhóm. Trong thang điểm VAS, mức độ hài lòng của người tham gia đạt điểm cao nhất ở tuần 10 trong nhóm PN và tuần 4 trong nhóm HA, sau đó giảm dần theo thời gian ở cả hai nhóm. Điểm GAIS, được đánh giá bởi các nhà nghiên cứu, cao hơn ở nhóm PN tại tuần 16, nhưng không có sự khác biệt đáng kể ở tuần 10 và 28.
Độ đàn hồi của da được đo bằng máy cutometer có xu hướng giảm theo thời gian. Trên khuôn mặt, tuổi có tương quan âm với R2, R5, và R7; đặc biệt, R7 có liên quan mạnh mẽ hơn đến sự lão hóa da (14). Khi nghiên cứu tiến triển từ mùa hè sang mùa đông, tỷ lệ cải thiện tổng thể ở cả hai nhóm đều giảm. Sau khi cố định các ảnh hưởng theo thời gian, tỷ lệ cải thiện của R2, R5, và R7 trong nhóm PN có xu hướng giảm chậm hơn về mặt thống kê. Độ ẩm của da, được đo bằng corneometer, cũng giảm dần, do nghiên cứu bắt đầu vào mùa hè và kết thúc vào mùa đông. Khi cố định các ảnh hưởng theo thời gian, sự khác biệt trong tỷ lệ cải thiện độ ẩm da ở nhóm PN có ý nghĩa thống kê. Hơn nữa, sự khác biệt giữa hai nhóm PN và HA dần trở nên rõ rệt theo thời gian.
Điều trị bằng PN cho thấy hiệu quả tốt hơn so với HA trong việc cải thiện độ sần của da và kích thước lỗ chân lông. Tỷ lệ cải thiện độ sần da ở nhóm HA giảm dần theo thời gian, trong khi đó, nhóm PN có xu hướng tăng và duy trì ổn định. Sự khác biệt đáng kể giữa hai nhóm đã được ghi nhận theo thời gian. Nhóm HA cho thấy sự cải thiện ngắn hạn do hiệu ứng thể tích vào tuần thứ 10 (sáu tuần sau lần điều trị cuối), nhưng sau đó giảm dần. Kết quả tương tự cũng được ghi nhận về kích thước lỗ chân lông. Trong nhóm PN, hiệu quả duy trì ổn định trong một thời gian, trong khi nhóm HA giảm liên tục, dẫn đến sự khác biệt đáng kể giữa hai nhóm vào tuần 16 và 28. Cuối cùng, không có sự khác biệt đáng kể về mật độ da giữa hai nhóm theo thời gian hoặc tại các thời điểm khác nhau.
HA có khả năng liên kết nước mạnh, giúp cung cấp độ ẩm cho da và cải thiện độ đàn hồi, cấu trúc, và độ săn chắc của da. Ngoài ra, HA cũng có thể kích thích nguyên bào sợi và tăng sản xuất collagen. Các nghiên cứu khác với việc tiêm chất làm đầy HA nội bì đã cho thấy kết quả tương tự, với sự cải thiện về độ đàn hồi và độ ẩm của da sớm nhất là hai tuần sau khi tiêm. Những thay đổi sớm này có thể bị ảnh hưởng bởi thể tích và khả năng liên kết nước của HA. Sự cải thiện về độ đàn hồi tiếp tục kéo dài đến tuần thứ 8 và 12 sau khi tiêm nhờ vào sự tăng sản xuất collagen.
PN cũng có mặt rộng rãi trong môi trường ngoại bào của cơ thể người và được sử dụng để điều chỉnh giai đoạn tái tạo của quá trình chữa lành vết thương. Các chuỗi PN có trọng lượng phân tử cao trong da dễ dàng liên kết với các phân tử nước để cung cấp độ ẩm và hoạt động như một chất “xử lý” các gốc tự do, có tác dụng chống oxy hóa và bảo vệ tế bào khỏi tổn thương do bức xạ UV. Các chuỗi PN này còn ảnh hưởng đến hoạt động chuyển hóa của nguyên bào sợi, các tế bào chính kiểm soát quá trình tái tạo các thành phần của da. PN góp phần vào quá trình tái tạo các thành phần chính tự thân của da như glycosaminoglycan, protein, glycoprotein và sợi liên kết, giúp duy trì chức năng sinh lý. Hơn nữa, sự phân hủy dần dần của các phân tử PN bởi enzym cho phép duy trì độ ẩm và hoạt động chống oxy hóa kéo dài, tạo ra điều kiện thuận lợi trong lớp bì để tái tạo. Việc sử dụng PN ngoại sinh cũng có thể đóng góp vào quá trình sản xuất glycosaminoglycan, protein, glycoprotein và sợi liên kết, giúp duy trì các chức năng sinh lý của chúng. Như vậy, PN chuỗi dài như Rejuran có hiệu quả trong việc cải thiện độ đàn hồi, độ ẩm và độ sần của da.
Hạn chế quan trọng nhất của nghiên cứu này là bắt đầu vào mùa hè, nhưng việc đánh giá hiệu quả chủ yếu diễn ra vào mùa đông. Các phép đo độ đàn hồi và độ ẩm của da có thể phản ứng nhạy cảm với sự thay đổi theo mùa. Thứ hai, bốn người tham gia đã bỏ cuộc ở lần đánh giá sau cùng vào tuần 28, có thể làm tăng tỷ lệ những người có hiệu quả tốt trong các đánh giá cuối cùng.
KẾT LUẬN
Nghiên cứu đã so sánh hiệu quả và tính an toàn của PN với HA bằng cách sử dụng nhiều phép đo khác nhau. PN cho thấy hiệu quả trong việc cải thiện độ ẩm của da, và độ đàn hồi giữa hai chất PN và HA là tương đương. Đặc biệt, về độ sần của da và kích thước lỗ chân lông, PN có hiệu quả vượt trội hơn so với HA. Chất làm đầy HA mang lại hiệu quả nhanh hơn, trong khi PN lại có tác dụng kéo dài hơn. Kết luận lại, PN và HA có cơ chế và tác động khác nhau trong việc trẻ hóa da, và việc tiêm kết hợp cả hai loại chất có thể mang lại hiệu quả hiệp đồng trong điều trị chống lão hóa da.
NGUỒN THAM KHẢO
- Sumino H, Ichikawa S, Abe M, et al. Effects of aging, menopause, and hormone replacement therapy on fore- arm skin elasticity in women. J Am Geriatr Soc. 2004;52(6): 945–949.
- Philipp-Dormston WG, Bergfeld D, Sommer BM, et al. Consensus statement on prevention and management of adverse effects following rejuvenation procedures with hyaluronic acid-based fillers. J Eur Acad Dermatol Venereol. 2017;31(7):1088–1095.
- Rhee do Y, Won CH, Chang SE, et al. Efficacy and safety of a new monophasic hyaluronic acid filler in the correction of nasolabial folds: a randomized, evaluator-blinded, split- face study. J Dermatolog Treat. 2014;25(5):448–452.
- Noh TK, Moon HR, Yu JS, et al. Effects of highly concen- trated hyaluronic acid filler on nasolabial fold correction: a 24-month extension study. J Dermatolog Treat. 2016;27(6): 510–514.
- Lemmens R, Vanduffel L, Teuchy H, et al. Regulation of proliferation of LLC-MK2 cells by nucleosides and nucleotides: the role of ecto-enzymes. Biochem J. 1996; 316(2):551–557.
- Rathbone MP, Middlemiss PJ, Gysbers JW, et al. Purine nucleosides and nucleotides stimulate proliferation of a wide range of cell types. In Vitro Cell Dev Biol – Animal. 1992;28(7-8):529–536.
- Galeano M, Bitto A, Altavilla D, et al. Polydeoxyribonucleotide stimulates angiogenesis and wound healing in the genetically diabetic mouse. Wound Repair Regen. 2008;16(2):208–217.
- Jin H, Seo J, Eun SY, et al. P2Y2 R activation by nucleoti- des promotes skin wound-healing process. Exp Dermatol. 2014;23(7):480–485.
- Sini P, Denti A, Cattarini G, et al. Effect of polydeoxyribo- nucleotides on human fibroblasts in primary culture. Cell Biochem Funct. 1999;17(2):107–114.
- Thellung S, Florio T, Maragliano A, et al. Polydeoxyribonucleotides enhance the proliferation of human skin fibroblasts: involvement of A2 purinergic receptor subtypes. Life Sci. 1999;64(18):1661–1674.
- Park KY, Seok J, Rho NK, et al. Long-chain polynucleotide filler for skin rejuvenation: efficacy and complications in five patients. Dermatol Ther. 2016;29(1):37–40.
- Messaraa C, Metois A, Walsh M, et al. Wrinkle and rough- ness measurement by the Antera 3D and its application for evaluation of cosmetic products. Skin Res Technol. 2018;24(3):359–366.
- Messaraa C, Metois A, Walsh M, et al. Antera 3D capabil- ities for pore measurements. Skin Res Technol. 2018;24(4): 606–613.
- Ryu HS, Joo YH, Kim SO, et al. Influence of age and regional differences on skin elasticity as measured by the Cutometer. Skin Res Technol. 2008;14(3):354–358.
- Streker M, Reuther T, Krueger N, et al. Stabilized hyalur- onic acid-based gel of non-animal origin for skin rejuven- ation: face, hand, and decolletage. J Drugs Dermatol. 2013;12:990–994.
- Wang F, Garza LA, Kang S, et al. In vivo stimulation of de novo collagen production caused by cross-linked hyalur- onic acid dermal filler injections in photodamaged human skin. Arch Dermatol. 2007;143(2):155–163.
- Jones IT, Vanaman Wilson MJ, Bolton J, et al. A single center, prospective, randomized, sham-controlled, double- blinded, split-face trial using microinjections of transpar- ent hyaluronic acid gel for cheek rejuvenation. Dermatol Surg. 2018;44:841–845.
- Roh NK, Kim MJ, Lee YW, et al. A split-face study of the effects of a stabilized hyaluronic acid-based gel of nonani- mal origin for facial skin rejuvenation using a stamp-type multineedle injector: a randomized clinical trial. Plast Reconstr Surg. 2016;137(3):809–816.
- Rathbone MP, Christjanson L, Deforge S, et al. Extracellular purine nucleosides stimulate cell division and morphogen- esis: pathological and physiological implications. Med Hypotheses. 1992;37(4):232–240.
- Cavallini M, Papagni M. Long chain polynucleotides gel and skin biorevitalization. J Plast Dermatology. 2007;3: 27–32.
- Avantaggiato A, Palmieri A, Carinci F, et al. Biostimulation and biorevitalization: effects on human skin fibroblasts. J Oral Maxillofac Surg. 2013;1:11.